
- Outeur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Laas verander 2025-01-22 16:55.
Een manier waarop dit dit doen, is deur twee belangrike reaksies genoem dehidrasie en hidrolise . Dehidrasie reaksies verbind monomere saam in polimere deur water vry te stel, en hidrolise breek polimere in monomere met behulp van 'n watermolekule. Monomere is net enkele eenheid molekules en polimere is kettings van monomere.
Verder, hoe is dehidrasie sintese en hidrolise verwant?
In dehidrasie sintese reaksies, word 'n watermolekule gevorm as gevolg van die generering van 'n kovalente binding tussen twee monomere komponente in 'n groter polimeer. In hidrolise reaksies, word 'n watermolekule verbruik as gevolg van die verbreking van die kovalente binding wat twee komponente van 'n polimeer bymekaar hou.
Mens kan ook vra, wat gebeur met water tydens dehidrasie sintese? Dehidrasie sintese is die proses om twee molekules, of verbindings, saam te voeg na die verwydering van water . Tydens 'n kondensasiereaksie, word twee molekules gekondenseer en water verlore gaan om 'n groot molekule te vorm. Dit is presies dieselfde proses wat plaasvind tydens a dehidrasie sintese.
Net so, wat is die verskil tussen dehidrasie en hidrolise?
Die verskil tussen dehidrasie sintese en hidrolise is dat in een, bindings gevorm word, terwyl in die ander bande word vernietig. Dehidrasie sintese bind molekules aan mekaar deur water te verwyder. In hidrolise , word water by die molekules gevoeg om daardie bindings op te los.
Wat is die gevolg van 'n dehidrasiereaksie?
In chemie, a dehidrasie reaksie is 'n chemiese stof reaksie wat die verlies van 'n watermolekule uit die reaktant behels. Daar is 'n ander soort reaksie , wat 'n kondensasie genoem word reaksie , wat breër gedefinieer word as a reaksie daardie resultate in verlies van 'n watermolekule.
Aanbeveel:
Hoe hou die woord matriks verband met mitochondria?
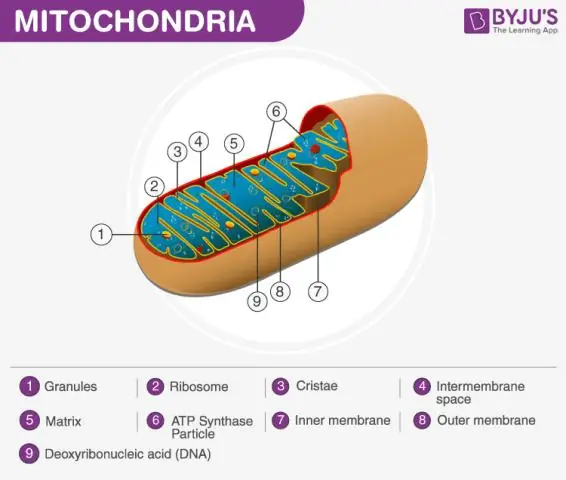
Die mitochondriale matriks Gedefinieer Die mitochondrion bestaan uit 'n buitenste membraan, 'n binnemembraan en 'n jelagtige materiaal wat die matriks genoem word. Hierdie matriks is meer viskeus as die sel se sitoplasma aangesien dit minder water bevat. Dit is 'n belangrike stap in sellulêre respirasie, wat energiemolekules genaamd ATP produseer
Hoe hou jou antwoord van vraag 1 verband met die Linnaeaanse klassifikasiestelsel?

Hoe hou jou antwoord van Vraag 1 verband met die Linnaeaanse klassifikasiestelsel? My antwoord uit vraag 1 hou verband met die Linnaen-klassifikasiestelsel deur eers die binne- en buitekant van die organisme te identifiseer. Daarna gebruik die Linneaanse klassifikasie kleur en grootte om die organisme te identifiseer
Hoe hou die wette van termodinamika en entropie verband?

Entropie is die verlies van energie wat beskikbaar is om werk te doen. 'n Ander vorm van die tweede wet van termodinamika stel dat die totale entropie van 'n sisteem óf toeneem óf konstant bly; dit neem nooit af nie. Entropie is nul in 'n omkeerbare proses; dit neem toe in 'n onomkeerbare proses
Watter van die volgende bevat hidrolitiese wat verband hou met hidrolise-ensieme?

Lisosome is membraan-omhulde kompartemente gevul met hidrolitiese ensieme wat gebruik word vir die beheerde intrasellulêre vertering van makromolekules. Hulle bevat ongeveer 40 tipes hidrolitiese ensieme, insluitend proteases, nukleases, glikosidases, lipases, fosfolipases, fosfatases en sulfatases
Hoe het organiese verbindings hul naam gekry. Hoe hou die woord verband met sy betekenis?
Hoe hou die woord verband met sy betekenis? Organiese verbindings kry sy naam van die aantal koolstofbindings. Die woord hou verband met die betekenis omdat dit te doen het met bindings in koolstofatome in organiese verbindings
