INHOUDSOPGAWE:
- Outeur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Laas verander 2025-01-22 16:55.
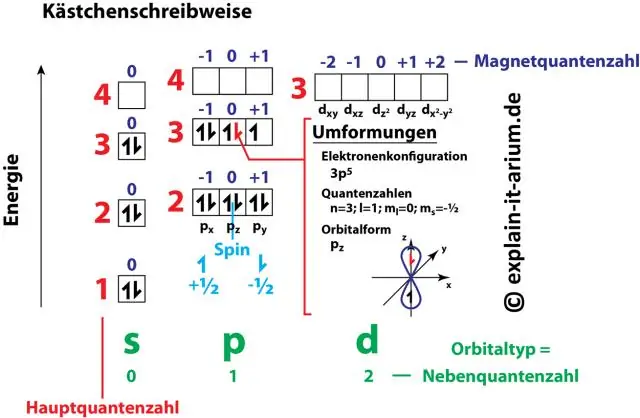
Die nommer en letterpare in 'n elektronkonfigurasie verteenwoordig twee van die elektron s'n vier kwantumgetalle . Hierdie kwantumgetalle vertel ons meer inligting oor die eienskappe van elektrone en hul orbitale. Die skoolhoof kwantumgetal (n) vertel ons 'n elektron s'n energievlak en die grootte daarvan.
Met betrekking tot hierdie, wat beskryf die vier kwantumgetalle oor 'n elektron?
Om heeltemal beskryf an elektron in 'n atoom, vier kwantumgetalle word benodig: energie (n), hoekmomentum (ℓ), magnetiese moment (mℓ), en spin (ms). Die eerste kwantum nommer beskryf die elektron dop, of energievlak, van 'n atoom.
Behalwe hierbo, wat is die 4 kwantumgetalle? Verduideliking: Die vier kwantumgetalle is die beginsel kwantumgetal, n, die hoekmomentum kwantumgetal ,l, die magnetiese kwantumgetal , ml, en die elektron spin kwantumgetal , mev.
Verder, hoe vind jy die kwantumgetal elektrone?
Hoe om die aantal elektrone met kwantumgetalle te bepaal
- Tel die volle orbitale.
- Voeg die elektrone by vir elke volle orbitaal.
- Identifiseer die subdop wat deur die hoekkwantumnommer aangedui word.
- Voeg die elektrone van die volledige subshells by.
- Voeg die elektrone van volle subskulpe by dié van volle orbitale.
- Vind die wettige waardes vir die magnetiese kwantumgetal.
Wat is 'n subshell?
A subdop is 'n onderafdeling van elektronskulpe geskei deur elektronorbitale. Subskulpe word s, p, d en f in 'n elektronkonfigurasie gemerk.
Aanbeveel:
Hoe hou die woord matriks verband met mitochondria?
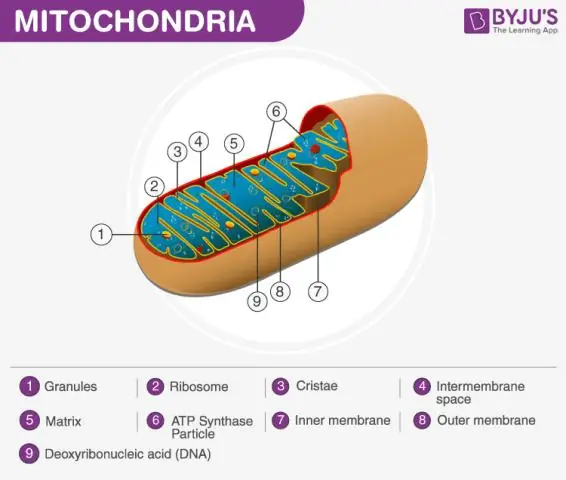
Die mitochondriale matriks Gedefinieer Die mitochondrion bestaan uit 'n buitenste membraan, 'n binnemembraan en 'n jelagtige materiaal wat die matriks genoem word. Hierdie matriks is meer viskeus as die sel se sitoplasma aangesien dit minder water bevat. Dit is 'n belangrike stap in sellulêre respirasie, wat energiemolekules genaamd ATP produseer
Hoe hou jou antwoord van vraag 1 verband met die Linnaeaanse klassifikasiestelsel?

Hoe hou jou antwoord van Vraag 1 verband met die Linnaeaanse klassifikasiestelsel? My antwoord uit vraag 1 hou verband met die Linnaen-klassifikasiestelsel deur eers die binne- en buitekant van die organisme te identifiseer. Daarna gebruik die Linneaanse klassifikasie kleur en grootte om die organisme te identifiseer
Hoe hou die Oos-Afrikaanse Skeur verband met plaattektoniek?

Die East African Rift Valley (EAR) is 'n ontwikkelende uiteenlopende plaatgrens in Oos-Afrika. Die Nubiese en Somaliese plate skei ook van die Arabiese plaat in die noorde en skep dus 'n 'Y'-vormige skeurstelsel. Hierdie plate sny mekaar in die Afar-streek van Ethiopië by wat bekend staan as 'n 'drievoudige aansluiting'
Hoe het organiese verbindings hul naam gekry. Hoe hou die woord verband met sy betekenis?
Hoe hou die woord verband met sy betekenis? Organiese verbindings kry sy naam van die aantal koolstofbindings. Die woord hou verband met die betekenis omdat dit te doen het met bindings in koolstofatome in organiese verbindings
Wat is natuurlike seleksie en hoe hou dit verband met afkoms met modifikasie?

Afkoms met modifikasie is die evolusionêre meganisme wat verandering in die genetiese kode van lewende organismes veroorsaak. Daar is drie meganismes vir sulke veranderinge en die vierde meganisme, natuurlike seleksie, bepaal watter afstammelinge oorleef om hul gene oor te dra, gebaseer op omgewingstoestande
