
- Outeur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Laas verander 2025-01-22 16:55.
Die entalpie van vorming vir 'n element in sy elementêre toestand sal altyd wees 0 omdat dit geen energie verg om 'n natuurlike verbinding te vorm nie. Wanneer 'n stof is gevorm van die mees stabiele vorm daarvan elemente , 'n verandering in entalpie Vind plaas.
Net so kan 'n mens vra, watter stowwe het 'n entalpie van vorming van nul?
Alle elemente in hul standaardtoestande (suurstofgas, vastestof koolstof in die vorm van grafiet , ens.) het 'n standaard-entalpie van vorming van nul, aangesien daar geen verandering by hul vorming betrokke is nie.
Gevolglik is die vraag, wat is die entalpie van vorming van water? Geselekteerde ATcT-entalpie van vorming gebaseer op weergawe 1.118 van die Thermochemical Network
| Spesie Naam | Formule | ΔfH°(298,15 K) |
|---|---|---|
| Water | H2O (cr, eq.press.) | -292.740 |
Dienooreenkomstig, hoekom is die standaardentalpie van vorming van diamant nie nul nie, alhoewel dit 'n element is?
Die standaard entalpie van formasie vir 'n element in sy standaard staat is NUL !!!! Dus, ΔH°f vir C (s, grafiet) is nul , maar die ΔH°f vir C (s, diamant ) is 2 kJ/mol. Dit is omdat grafiet die standaard staat vir koolstof, nie diamant nie.
Wat beteken dit as Delta h nul is?
Hulle kan slegs veranderinge in entalpie meet. Wanneer entalpie positief is en delta H is groter as nul , hierdie beteken dat 'n sisteem hitte geabsorbeer het. Dit word 'n endotermiese reaksie genoem. Wanneer entalpie negatief is en delta H is minder as nul , hierdie beteken dat 'n sisteem hitte vrygestel het. Dit word 'n eksotermiese reaksie genoem.
Aanbeveel:
Hoekom is die EMK nul wanneer die spoel deur die presiese middelpunt van die magneet beweeg?
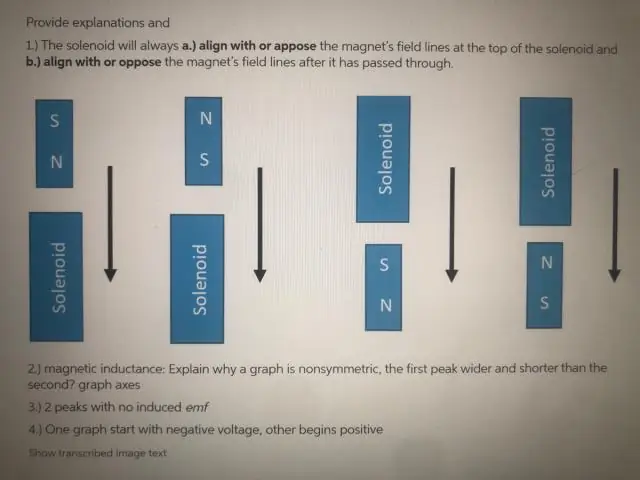
Die emk is net nul vir 'n oomblik as die magneet deur die presiese middelpunt van die spoel beweeg. Dit is omdat die effek van die N-pool aan die een kant van die magneet op daardie kant van die spoel presies uitgekanselleer word deur die effek van die S-pool van die magneet aan die ander kant van die spoel
Wat is die standaard entalpie van vorming vir swaeldioksied?

Om na te gaan, moet dit (−296.81±0.20) kJ/mol wees. Jy moet NIST meer gereeld gebruik. Ek het eintlik −310.17 kJ/mol gekry. Jy moet eers ΔH∘f vir SO3(g) opsoek
Wat is die entalpie van vorming van Cao?

Tabel van Vormingsverhitte Verbinding ΔHf (kJ/mol) CaCO3 -1207.0 CaO(s) -635.5 Ca(OH)2(s) -986.6 CaSO4(s) -1432.7
Hoe vergelyk die oorvloed van elemente op Aarde met die oorvloed van elemente in mense?

Suurstof is die volopste element op aarde sowel as by mense. Die oorvloed van elemente wat organiese verbindings vorm, neem toe by mense, terwyl die oorvloed van metalloïede op Aarde toeneem. Die elemente wat volop op Aarde is, is noodsaaklik om lewe te onderhou
Hoe vind jy die standaard entalpie van vorming van verbranding?

Die standaard-entalpie van reaksie (ΔHorxn) kan bereken word uit die som van die standaard-entalpieë van vorming van die produkte (elk vermenigvuldig met sy stoïgiometriese koëffisiënt) minus die som van die standaard-entalpieë van vorming van die reaktante (elk vermenigvuldig met sy stoïgiometriese koëffisiënt)-die “produkte
