
- Outeur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Laas verander 2025-01-22 16:55.
1 Antwoord. Die standaard entalpie verandering van formasie, of Δ H ∘f, van magnesiumoksied sal -601.6 kJ/mol wees.
Op hierdie manier, wat is die standaard entalpie van vorming van MgO?
-601,7 kJ/mol
Net so, hoe bereken ek delta H? Gebruik die formule ∆ H = m x s x ∆T om op te los. Sodra jy m, die massa van jou reaktante, s, die spesifieke hitte van jou produk, en ∆T, die temperatuurverandering vanaf jou reaksie het, is jy bereid om die entalpie van reaksie te vind. Sluit eenvoudig jou waardes in die formule ∆ H = m x s x ∆T en vermenigvuldig om op te los.
Hierbenewens, is MgO en HCl eksotermies?
Kanika Gupta. Magnesiumoksied ( MgO ) word geproduseer wanneer magnesium (Mg) by hoë temperature brand, wat 'n helder, warm vlam produseer. Wanneer vaste Mg reageer met HCl ( soutsuur ), magnesiumchloried (MgCl2), waterstofgas en hitte word geproduseer. Hitte word geproduseer omdat die reaksie is eksotermies.
Hoeveel gram magnesiumoksied sal geproduseer word as die hitte wat uit die verbranding van magnesium ontwikkel is kJ was?
18 molMg. 18molMg x 24,3 g /molMg = 4.37gMg x -108kJ 7.25 g MgO sou geproduseer word as die hitte uit die verbranding van Mg ontwikkel het was -108kJ. Dit is bereken deur 'n verhouding te skep tussen die mol wat gebruik word en die hitte ontwikkel het , en vermenigvuldig dan daardie resultaat met die molêre massa van MgO.
Aanbeveel:
Wat is die naam van die chemiese stof waar die energie tydens die eerste fase van fotosintese gestoor word?
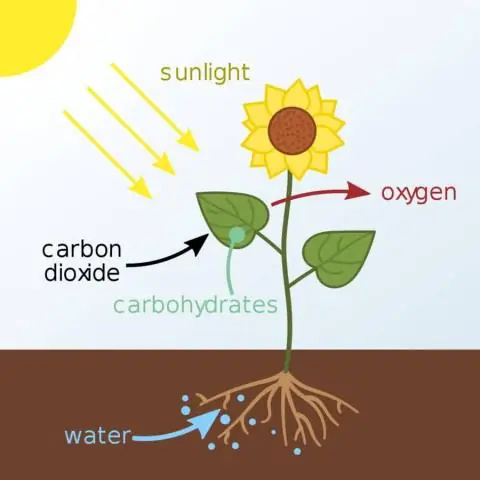
Die ligafhanklike reaksies gebruik ligenergie om twee molekules te maak wat nodig is vir die volgende stadium van fotosintese: die energiebergingsmolekule ATP en die gereduseerde elektrondraer NADPH. By plante vind die ligreaksies plaas in die tilakoïedmembrane van organelle wat chloroplaste genoem word
Wat is die korrekte volgorde van die ekologiese hiërargie van die kleinste na die grootste?

Opsomming Vlakke van organisasie in ekologie sluit die bevolking, gemeenskap, ekosisteem en biosfeer in. 'n Ekosisteem is al die lewende dinge in 'n gebied wat in wisselwerking is met al die abiotiese dele van die omgewing
Wat suggereer die verspreiding van die seebodem op die ouderdom van die seebodem?
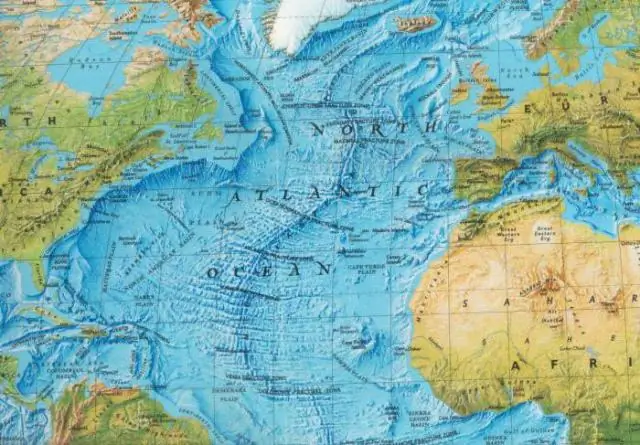
Die jongste kors van die seebodem kan gevind word naby die seebodemverspreidingsentrums of middel-oseaan-rante. Soos die plate uitmekaar skei, styg magma van onder die aarde se oppervlak af om die leë leemte in te vul. In wese is oseaniese plate meer vatbaar vir subduksie namate hulle ouer word
Wat is die naam van die ensiem wat die sintese van die mRNA-streng kataliseer?
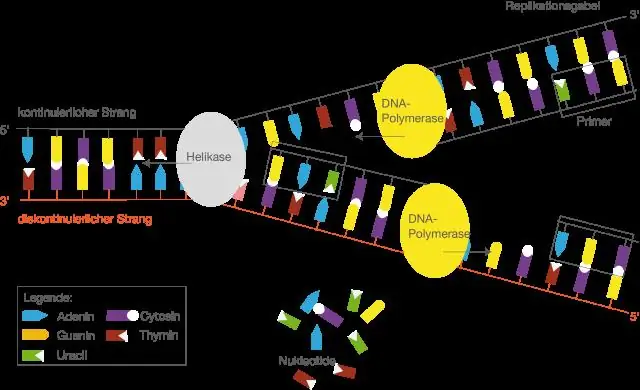
MRNA is "boodskapper" RNA. mRNA word in die kern gesintetiseer deur die nukleotiedvolgorde van DNA as 'n sjabloon te gebruik. Hierdie proses vereis nukleotiedtrifosfate as substrate en word deur die ensiem RNA-polimerase II gekataliseer. Die proses om mRNA van DNA te maak, word transkripsie genoem, en dit vind in die kern plaas
Wat is die oksidasietoestand van magnesium in MgO?

In die vorming van magnesiumoksied uit magnesium en suurstof het die magnesiumatome twee elektrone verloor, of die oksidasiegetal het van nul tot +2 toegeneem
