
INHOUDSOPGAWE:
- Outeur Miles Stephen stephen@answers-science.com.
- Public 2024-01-18 08:12.
- Laas verander 2025-01-22 16:55.
Bepalings in hierdie stel (10)
- Die eenvoudigste formule vir 'n kovalente verbinding is sy.
- Die anioon wat uit 'n suurstofatoom gevorm word, word 'n genoem.
- Fe O word yster(III)oksied genoem omdat dit bevat.
- Dit is moontlik vir verskillende kovalente verbindings om dieselfde empiriese formule te hê, want empiriese formules verteenwoordig.
Hiervan, wat is die formule vir 'n kovalente verbinding?
Benoem binêre (twee-element) kovalente verbindings is soortgelyk aan die naam van eenvoudige ioniese verbindings . Die eerste element in die formule word eenvoudig gelys deur die naam van die element te gebruik. Die tweede element word benoem deur die stam van die elementnaam te neem en die agtervoegsel -ide by te voeg.
Gevolglik is die vraag, hoe skryf jy formules vir verbindings? Om die empiriese formule vir 'n ioniese verbinding te skryf:
- Identifiseer die katioon.
- Skryf die korrekte formule en laai vir die katioon.
- Identifiseer die anioon.
- Skryf die korrekte formule en laai vir die anioon.
- Kombineer die katioon en anioon om 'n elektries neutrale verbinding te produseer.
Om ook te weet is, wat is 'n voorbeeld van 'n kovalente verbinding?
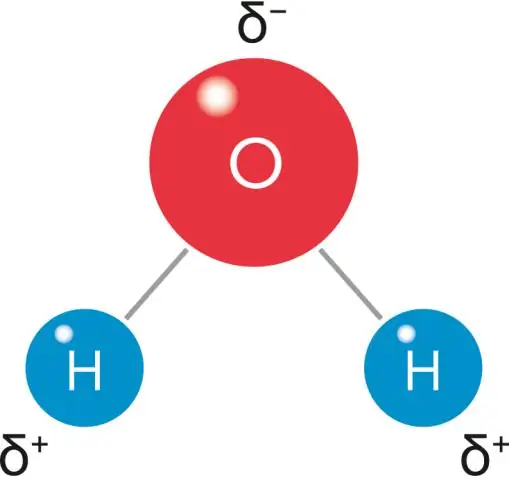
A kovalent binding vorm tussen twee nie-metale deur elektrone te deel, dus 'n voorbeeld kan "Water, H2O" wees, aangesien dit gevorm word deur die deel van elektrone van waterstof en suurstof (wat albei nie-metale is). En nog een voorbeeld van 'n kovalent binding coud "Koolstofdioksied, CO2".
Wat is 'n ander naam vir 'n kovalente verbinding?
A kovalent binding, ook genoem 'n molekulêre binding, is 'n chemiese binding wat die deling van elektronpare tussen atome behels. Hierdie elektronpare staan bekend as gedeelde pare of bindingspare, en die stabiele balans van aantrekkings- en afstootkragte tussen atome, wanneer hulle elektrone deel, staan bekend as kovalent binding.
Aanbeveel:
Wat is die eenvoudigste vorm vir 6 20?

Vereenvoudig 6/20 tot die eenvoudigste vorm. Aanlyn vereenvoudig breuke sakrekenaar om 6/20 vinnig en maklik tot die laagste terme te verminder. 6/20 Vereenvoudigde Antwoord: 6/20 = 3/10
Wat is die naam van die verbinding met die formule CuCrO4?
Koper(II) Chromaat CuCrO4 Molekulêre Gewig --EndMemo
Hoe skryf jy die formule vir 'n verbinding wat 'n poliatomiese ioon bevat?
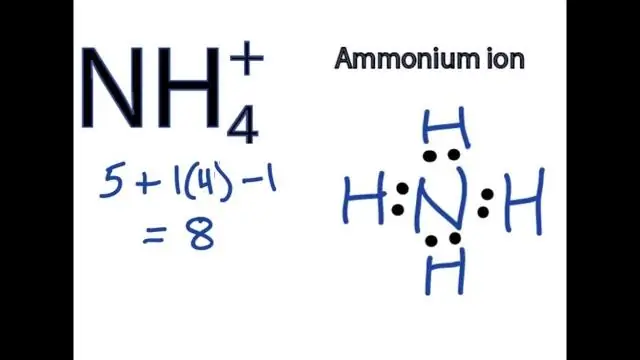
Om formules te skryf vir verbindings wat poliatomiese ione bevat, skryf die simbool vir die metaalioon gevolg deur die formule vir die poliatomiese ioon en balanseer die ladings. Om 'n verbinding te noem wat 'n poliatomiese ioon bevat, noem eers die katioon en dan die anioon
Wat is die som van die atoommassas van al die atome in 'n formule vir 'n verbinding?

Die formulemassa van 'n stof is die som van die gemiddelde atoommassas van elke atoom wat in die chemiese formule voorgestel word en word uitgedruk in atoommassa-eenhede. Die formulemassa van 'n kovalente verbinding word ook die molekulêre massa genoem
Wat sê die chemiese formule vir magnesiumchloried oor die verbinding?

Die chemiese formule van magnesiumchloried is _MgCl2. Aangesien magnesium aan die 2de groep in die periodieke tabel behoort en +2 ioon vorm en chloor aan halogeenfamilie behoort en -1 ioon vorm. Hulle reageer dus om MgCl2 te vorm. Magnesium kombineer met 2 Cl-atome om sy oktaat te voltooi
