
- Outeur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Laas verander 2025-01-22 16:55.
In nul - bestel kinetika , die koers van 'n reaksie doen nie afhang van die substraatkonsentrasie nie. Die t 1 /2 formule vir 'n nul-orde reaksie stel voor die helfte - lewe hang af van die hoeveelheid aanvanklike konsentrasie en tempo konstante.
Vervolgens kan 'n mens ook vra, wat is die halfleeftyd vir 'n nul-orde reaksie?
96 sekondes
Ook, hoe vind jy die halfleeftyd van 'n tempokonstante? Strategie:
- Gebruik Vergelyking 3 om die halfleeftyd van die reaksie te bereken.
- Vermenigvuldig die aanvanklike konsentrasie met 1/2 tot die mag wat ooreenstem met die aantal halfleeftye om die oorblywende konsentrasies na daardie halfleeftye te verkry.
- Trek die oorblywende konsentrasie van die aanvanklike konsentrasie af.
Wat dit betref, hoekom is die halfleeftyd van 'n eerste-orde reaksie konstant?
Met ander woorde, die aanvanklike konsentrasie van die reaktant het geen invloed op die helfte - lewe van die reaksie , d.w.s. die helfte - lewe is konstant ongeag die konsentrasie van die reaktant.
Hang die halfleeftyd van 'n nul-orde reaksie af van die aanvanklike konsentrasie van die reaktant?
Vandaar, uit die bogenoemde vergelyking ons kan kom tot die gevolgtrekking dat die halfleeftyd van 'n nul-orde reaksie hang af aan aanvanklike konsentrasie van reagerende spesies en die tempokonstante, k. Dit is direk eweredig aan aanvanklike konsentrasie van die reaktant terwyl dit omgekeerd eweredig is aan die tempokonstante, k.
Aanbeveel:
Hoe hou die struktuur van koolstof verband met die verskeidenheid makromolekules wat in lewende dinge voorkom?
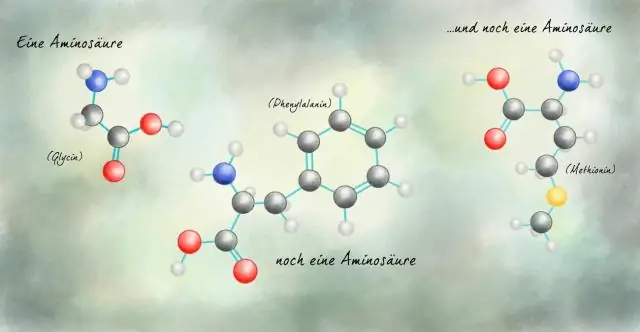
Die koolstofatoom het unieke eienskappe wat dit toelaat om kovalente bindings aan soveel as vier verskillende atome te vorm, wat hierdie veelsydige element ideaal maak om as die basiese strukturele komponent, of "ruggraat" van die makromolekules te dien
Hoe dink jy hou die samehangende aard van water verband met die verdamping daarvan?

Kohesie van water Voordat dit oorloop, vorm die water 'n koepelagtige vorm bo die rand van die glas. Kohesie verwys na die aantrekking van molekules vir ander molekules van dieselfde soort, en watermolekules het sterk kohesiekragte danksy hul vermoë om waterstofbindings met mekaar te vorm
Hoe hou die struktuur van die vakuool verband met sy funksie?

Vakuole is membraangebonde sakkies binne die sitoplasma van 'n sel wat op verskeie maniere funksioneer. In volwasse plantselle is vakuole geneig om baie groot te wees en is dit uiters belangrik in die verskaffing van strukturele ondersteuning, sowel as om funksies te dien soos berging, afvalverwydering, beskerming en groei
Hoe hou die aftrekking van heelgetalle verband met die optel van heelgetalle?

Antwoord en verduideliking: Om heelgetalle op te tel beteken om heelgetalle met dieselfde tekens by te tel, terwyl heelgetalle aftrek beteken om die heelgetalle van teenoorgestelde tekens op te tel
Hoe sal produk wat per minuut geproduseer word verband hou met die tempo van 'n ensiemgekataliseerde reaksie?
Vir 'n ensiemgekataliseerde reaksie word die tempo gewoonlik uitgedruk in die hoeveelheid produk wat per minuut geproduseer word. By lae temperatuur verhoog verwarming gewoonlik die tempo van 'n ensiemgekataliseerde reaksie omdat die reaktante meer energie het en makliker die aktiveringsenergievlak kan bereik
