
- Outeur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Laas verander 2025-06-01 05:03.
Water, 'n Polar Bond
Waterstof het 'n elektronegatiwiteit van 2.0, terwyl suurstof 'n elektronegatiwiteit van 3.5 het. Die verskil in elektronegatiwiteite is 1,5, wat beteken dat water 'n polêre kovalente molekule is
Verder, wat is elektronegatiwiteit met voorbeeld?
Elektronegatiwiteit Voorbeeld Die chlooratoom het 'n hoër elektronegatiwiteit as die waterstofatoom, dus sal die bindingselektrone nader aan die Cl as aan die H in die HCl-molekule wees. Die elektrone in die kovalente binding word gelykop tussen die twee suurstofatome gedeel.
Net so, wat beteken die verskil in elektronegatiwiteit? Elektronegatiwiteit is 'n maatstaf van 'n atoom se vermoë om die gedeelde elektrone van 'n kovalente binding na homself aan te trek. As die verskil in elektronegatiwiteit groot genoeg is, sal die elektrone glad nie gedeel word nie; die meer elektronegatief atoom sal hulle "vat" wat lei tot twee ione en 'n ioniese binding.
Behalwe dit, wat is die elektronegatiwiteit van nacl?
Natriumchloried is ionies gebind. 'n Elektron het van natrium na chloor oorgedra. Natrium het 'n elektronegatiwiteit van 1.0, en chloor het 'n elektronegatiwiteit van 3.0. Dit is 'n elektronegatiwiteit verskil van 2.0 (3.0 - 1.0), wat die binding tussen die twee atome baie, baie polêr maak.
Wat is die beste definisie van elektronegatiwiteit?
Elektronegatiwiteit is 'n maatstaf van die neiging van 'n atoom om 'n bindingspaar elektrone aan te trek. Die Pauling-skaal is die algemeenste. Fluoor (die meeste elektronegatief element) word 'n waarde van 4.0 toegeken, en waardes wissel tot sesium en francium wat die minste is elektronegatief op 0.7.
Aanbeveel:
Wat is die naam van die chemiese stof waar die energie tydens die eerste fase van fotosintese gestoor word?
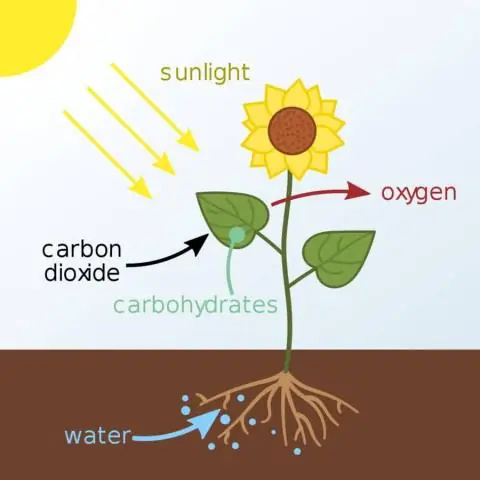
Die ligafhanklike reaksies gebruik ligenergie om twee molekules te maak wat nodig is vir die volgende stadium van fotosintese: die energiebergingsmolekule ATP en die gereduseerde elektrondraer NADPH. By plante vind die ligreaksies plaas in die tilakoïedmembrane van organelle wat chloroplaste genoem word
Hoekom het halogene hoë elektronegatiwiteit?

As gevolg van hul hoë effektiewe kernlading, is halogene hoogs elektronegatief. Daarom is hulle hoogs reaktief en kan 'n elektron verkry deur reaksie met ander elemente. Halogene kan in voldoende hoeveelhede skadelik of dodelik wees vir biologiese organismes
Wat is die korrekte volgorde van die ekologiese hiërargie van die kleinste na die grootste?

Opsomming Vlakke van organisasie in ekologie sluit die bevolking, gemeenskap, ekosisteem en biosfeer in. 'n Ekosisteem is al die lewende dinge in 'n gebied wat in wisselwerking is met al die abiotiese dele van die omgewing
Wat is die neiging in elektronegatiwiteit wat 'n groep afneem?

Dus, soos jy 'n groep op die periodieke tabel afbeweeg, verminder die elektronegatiwiteit van 'n element omdat die verhoogde aantal energievlakke die buitenste elektrone baie ver van die trekkrag van die kern plaas. Elektronegatiwiteit neem toe soos jy van links na regs oor 'n tydperk op die periodieke tabel beweeg
Wat is die naam van die ensiem wat die sintese van die mRNA-streng kataliseer?
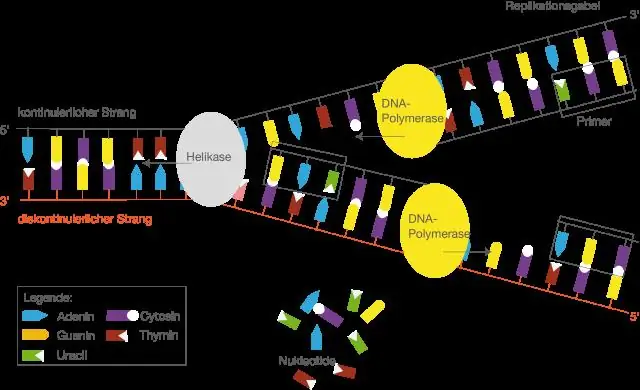
MRNA is "boodskapper" RNA. mRNA word in die kern gesintetiseer deur die nukleotiedvolgorde van DNA as 'n sjabloon te gebruik. Hierdie proses vereis nukleotiedtrifosfate as substrate en word deur die ensiem RNA-polimerase II gekataliseer. Die proses om mRNA van DNA te maak, word transkripsie genoem, en dit vind in die kern plaas
