
INHOUDSOPGAWE:
- Outeur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Laas verander 2025-01-22 16:55.
An ioniese verbinding is 'n reus struktuur van ione . Die ione het 'n gereelde, herhalende reëling genoem 'n ioniese rooster . Hierdie is hoekom solied ioniese verbindings vorm kristalle met gereelde vorms.
Buitendien, hoekom bestaan ioniese verbindings in 'n kristallyne rooster?
Die eienskappe van ioniese verbindings volg uit orde kristalrooster rangskikking van styfgebonde gelaaide deeltjies waaruit hulle bestaan. Ioniese verbindings geneig om hoë smelt- en kookpunte te hê, want die aantrekkingskrag tussen ione in die rooster is baie sterk.
Net so, wat is ioniese rooster? An ioniese verbinding bestaan uit katione en anione in a rooster struktuur. Die ioniese rooster struktuur word bymekaar gehou deur die elektrostatiese aantrekkingskragte tussen die teenoorgestelde gelaaide ione . 'n Metaal of metaallegering bestaan uit metaalkatione en 'n see van gedelokaliseerde elektrone.
Hierin, is alle ioniese verbindings kristallyn?
Individueel ione binne 'n ioniese verbinding het gewoonlik veelvuldige naaste bure, word dus nie as deel van molekules beskou nie, maar eerder as deel van 'n aaneenlopende driedimensionele netwerk, gewoonlik in 'n kristallyn struktuur. Ioniese verbindings het tipies hoë smelt- en kookpunte, en is hard en bros.
Wat is die 4 kenmerke van ioniese verbindings?
Hier is 'n kort lys van hoofeienskappe:
- Hulle vorm kristalle.
- Hulle het hoër entalpieë van samesmelting en verdamping as molekulêre verbindings.
- Hulle is moeilik.
- Hulle is bros.
- Hulle het hoë smeltpunte en ook hoë kookpunte.
- Hulle gelei elektrisiteit maar slegs wanneer hulle in water opgelos word.
Aanbeveel:
Wat is die toestand van ioniese verbindings by kamertemperatuur?

Kovalente bindings vs Ioniese bindings Kovalente bindings Ioniese bindings Toestand by kamertemperatuur: Vloeistof of gasvormig Vastestof Polariteit: Laag Hoog
Wat is die strukturele eenhede waaruit ioniese verbindings bestaan en hoe word hulle benoem?

Vir binêre ioniese verbindings (ioniese verbindings wat slegs twee tipes elemente bevat), word die verbindings benoem deur die naam van die katioon eerste te skryf gevolg deur die naam van die anioon. Byvoorbeeld, KCl, 'n ioniese verbinding wat K+ en Cl-ione bevat, word kaliumchloried genoem
Waarom los ioniese verbindings maklik in water op?

Om 'n ioniese verbinding op te los, moet die watermolekules die ione kan stabiliseer wat voortspruit uit die verbreking van die ioniese binding. Hulle doen dit deur die ione te hidreer. Water is 'n polêre molekule. Wanneer jy 'n ioniese stof in water plaas, trek die watermolekules die positiewe en negatiewe ione van die kristal aan
Hoe noem jy voorbeelde van ioniese verbindings?

Vir binêre ioniese verbindings (ioniese verbindings wat slegs twee tipes elemente bevat), word die verbindings benoem deur die naam van die katioon eerste te skryf gevolg deur die naam van die anioon. Byvoorbeeld, KCl, 'n ioniese verbinding wat K+ en Cl-ione bevat, word kaliumchloried genoem
Hoe skryf jy formules vir binêre ioniese verbindings?
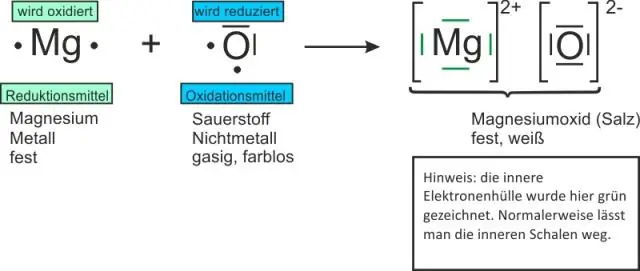
Formules vir binêre verbindings begin met die metaal gevolg deur die nie-metaal. Positiewe en negatiewe ladings moet mekaar uitkanselleer. Ioniese saamgestelde formules word geskryf deur die laagste verhouding van ione te gebruik
