
- Outeur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Laas verander 2025-01-22 16:55.
Die rede vir die hoë smelting en kook temperature is die waterstofbinding tussen water molekules wat veroorsaak dat hulle aan mekaar vashou en weerstaan om uitmekaar getrek te word, wat gebeur wanneer ys smelt en water kook om 'n gas te word.
Buitendien, hoekom is dit belangrik dat water 'n hoër kookpunt het?
Water het sterk waterstofbindings tussen molekules. Hierdie bindings verg baie energie voordat hulle sal breek. Dit lei tot water met 'n hoër kookpunt as as daar net swakker dipool-dipoolkragte was. Water is in staat om infrarooi straling (hitte) van die son te absorbeer.
Verder, wat is hoë smelt- en kookpunt? Metale het die hoogste kookpunt en smeltpunte omdat hulle die sterkste chemiese bindings het wat metaalagtig is. Die meeste van die metale is teenwoordig in die vaste toestand in normale kamer temperatuur . Dit is omdat die molekules deur sterk molekulêre krag van metaalbinding bymekaar gehou word om 'n harde roosterstruktuur te vorm.
As jy dit in ag neem, het water 'n hoë of lae smeltpunt?
Water molekules is aan mekaar geheg deur hidogeenbindings wat effens sterker is as van dar Waals-krag; daarom is dit vloeibaar by kamertemperatuur. Tog het dit baie geverg laag energie om die H-bindingsenergie uit te skakel in vergelyking met die ioniese bindings. Daarom is sy smeltpunt is relatief laer.
Is water dipool dipool?
Water het 'n sterk waterstofbinding dipool - dipool intermolekulêre kragte wat gee water 'n hoë oppervlakspanning en 'n hoë verdampingshitte en dit maak dit 'n sterk oplosmiddel.
Aanbeveel:
Hoe verskil water onder sy smeltpunt en bokant dit?

Hoe verskil water onder sy smeltpunt en bokant dit? Daaronder bly dit naby mekaar en hulle bons van mekaar af. Bo kom die molekules selfs nader as onder. Die kook-/kondensasiepunt van water is 373K
Waarom het etielalkohol 'n hoër kookpunt as metielalkohol?

Etanol het 'n hoër kookpunt as metanol. Gevolglik word meer energie benodig om die intermolekulêre kragte te oorkom, wat lei tot die toename in kook-/smeltpunte
Het water 'n lae smeltpunt?

Water het eintlik nie 'n lae smeltpunt in vergelyking met ander kovalente verbindings nie. Die meeste van die lae molêre massa kovalente verbindings is gasvormig by kamertemperatuur terwyl water vloeibaar is. Kovalente bindings is sterk genoeg, maar hulle is beperk tot individuele molekules nie tot die hele stuk van die verbinding nie
Hoekom het water 'n hoë smeltpunt?
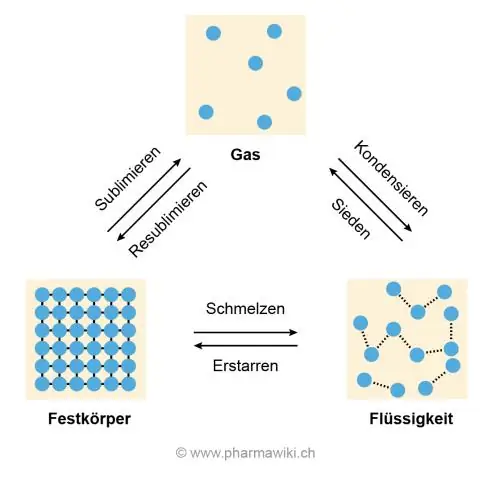
Die rede vir die hoë smelt- en kooktemperature is die waterstofbinding tussen watermolekules wat veroorsaak dat hulle aan mekaar vassit en nie uitmekaar getrek word nie, wat gebeur wanneer ys smelt en water kook om 'n gas te word
Waarom het natrium 'n hoë smeltpunt?

Natriumchloried het 'n hoë smeltpunt as gevolg van die sterk elektrostatiese aantrekkingskrag tussen sy positiewe en negatiewe ione; dit verg meer hitte-energie om te oorkom. Dit het ook 'n reuse-roosterstruktuur, wat beteken dat dit miljoene sterk ioniese bindings bevat
