
- Outeur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Laas verander 2025-01-22 16:55.
Clausius - Clapeyron-vergelyking - n voorbeeld.
Bereken die molfraksie van water (die oplosmiddel).
- Xoplosmiddel = nwater / (nglukose + nwater).
- Molêre massa van water is 18 g/mol, en vir glukose is dit 180,2 g/mol.
- water = 500/18 = 27.70 mol.
- glukose = 100 / 180.2 = 0.555 mol.
- Xoplosmiddel = 27.70 / (27.70 + 0.555) = 0.98.
Net so, vra mense, wat verteenwoordig die Clausius Clapeyron-vergelyking?
Meer algemeen die Clausius - Clapeyron-vergelyking het betrekking op die verband tussen die druk en temperatuur vir toestande van ewewig tussen twee fases. Die twee fases kan damp en vaste stof wees vir sublimasie of vastestof en vloeistof vir smelt.
Mens kan ook vra, waarvoor staan C in die Clausius Clapeyron-vergelyking? (1) waar ln P is die natuurlike logaritme van die dampdruk, ∆Hvap is die hitte van verdamping, R is die universele gaskonstante (8.31 J·K-1mol-1), T die absolute temperatuur, en C 'n konstante (nie verwant aan hittekapasiteit nie).
Om ook te weet is, wat is die Clausius Clapeyron-vergelyking en hoekom is dit belangrik?
Clausius - Clapeyron-vergelyking word vir die volgende doeleindes gebruik: Om die dampdruk by enige temperatuur te skat. Om die hitteverdamping van fase-oorgang te skat vanaf die dampdruk gemeet by twee temperature.
Wat is die vergelyking vir verdampingswarmte?
Gebruik die formule q = m·ΔHv waarin q = hitte energie, m = massa en ΔHv = hitte van verdamping.
Aanbeveel:
Hoe bereken jy standaardafwyking van PMP?

Die formule wat in die PMBOK vir standaardafwyking gebruik word, is eenvoudig. Dit is net (P-O)/6. Dit is die pessimistiese aktiwiteitskatting minus die optimistiese aktiwiteitskatting gedeel deur ses. Die probleem is dat hierdie vorm of vorm geensins 'n mate van standaardafwyking produseer nie
Hoe bereken jy die omtrek van die Aarde op sy breedtegraad?

Omtrek van 'n sirkel is gelyk aan 2πr waar r sy radius is. Op die Aarde is die omtrek van die sfeer op 'n gegewe breedtegraad 2πr(cos θ) waar θ is die breedtegraad en r is die radius van die Aarde by die ewenaar
Hoe bereken jy frekwensie uit frekwensie en persentasie?
Om dit te doen, deel die frekwensie deur die totale aantal resultate en vermenigvuldig met 100. In hierdie geval is die frekwensie van die eerste ry 1 en die totale aantal resultate is 10. Die persentasie sal dan 10,0 wees. Die laaste kolom is Kumulatiewe persentasie
Hoe bereken jy potensiële daling in 'n stroombaan?
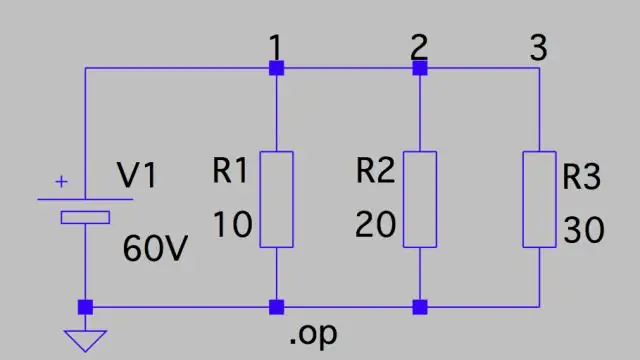
Spanningsval: Parallelle stroombaan Dit beteken dat die spanningsval oor elkeen net die totale spanning van die stroombaan is gedeel deur die aantal weerstande in die stroombaan, of 24 V/3 = 8 V
Hoe bereken jy hoe ver 'n voorwerp sal beweeg?

Horisontale afstand afgelê kan uitgedruk word as x = Vx * t, waar t die tyd is. Vertikale afstand vanaf die grond word beskryf deur die formule y = h + Vy * t – g * t² / 2, waar g die swaartekragversnelling is
