INHOUDSOPGAWE:
- Outeur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Laas verander 2025-01-22 16:55.
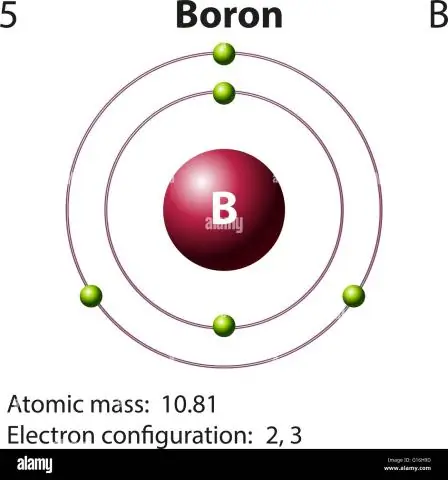
Vir boor sal hierdie vergelyking soos volg lyk:
- 5 protone + 5 neutrone = 10 atoommassa eenhede (AMU) of, vir die meer algemeen voorkomende boor isotoop (ongeveer.
- 5 protone + 6 neutrone = 11 AMU.
As jy dit in ag neem, wat is atoommassa van boor?
10.811 u
Ook, hoe bereken jy die atoommassa van neon? 20.1797 u
Mense vra ook, hoe bereken jy atoommassa?
Om bereken die atoommassa van 'n enkeling atoom van 'n element, tel die by massa van protone en neutrone. Voorbeeld: Vind die atoommassa van 'n isotoop van koolstof wat 7 neutrone het. Jy kan uit die periodieke tabel sien dat koolstof 'n atoom getal van 6, wat sy aantal protone is.
Wat het 'n massa van 1 amu?
'n Atoommassa-eenheid (gesimboliseer AMU of amu) word gedefinieer as presies 1/12 die massa van 'n atoom van koolstof-12. Die koolstof-12 (C-12) atoom het ses protone en ses neutrone in sy kern. In onakkurate terme is een AMU die gemiddelde van die proton rusmassa en die neutron rusmassa.
Aanbeveel:
Wat is die gemiddelde atoommassa van 'n atoom?

Die gemiddelde atoommassa van 'n element is die som van die massas van sy isotope, elk vermenigvuldig met sy natuurlike oorvloed (die desimale wat geassosieer word met persentasie atome van daardie element wat van 'n gegewe isotoop is). Gemiddelde atoommassa = f1M1 + f2M2 +
Hoe bereken jy die gemiddelde atoommassa van strontium?

Dus, ons bereken dit deur die geweegde massa van elk van die isotope te neem en hulle bymekaar te tel. Dus, vir die eerste massa, vermenigvuldig ons 0,50% van 84 (amu - atoommassa-eenhede) = 0,042 amu, en voeg dit by 9,9% van 86 amu = 8,51 amu, ensovoorts
Hoe word die gemiddelde atoommassa op die periodieke tabel bepaal?

Die gemiddelde atoommassa vir 'n element word bereken deur die massas van die element se isotope op te som, elk vermenigvuldig met sy natuurlike oorvloed op Aarde. Wanneer enige massaberekeninge gedoen word wat elemente of verbindings insluit, gebruik altyd gemiddelde atoommassa, wat op die periodieke tabel gevind kan word
Het al die atome van magnesium dieselfde atoommassa?

A: Magnesium, in sy elementêre vorm, het 12 protone en 12 elektrone. Die neutrone is 'n ander saak. Magesium se gemiddelde atoommassa is 24.305 atoommassa-eenhede, maar geen magnesiumatoom het presies hierdie massa
Hoe bereken jy atoommassa praktykprobleme?

VIDEO Hoe los jy dan atoommassaprobleme op? Om bereken die atoommassa van 'n enkele atoom van 'n element, tel die by massa van protone en neutrone. Voorbeeld: Vind die atoommassa van 'n isotoop van koolstof wat 7 neutrone het. Jy kan uit die periodieke tabel sien dat koolstof 'n atoom getal van 6, wat sy aantal protone is.
